当研究室の大学院生、竹尾沙優里さん(博士後期課程3年)、田口佳紀くん(博士後期課程3年)、飯尾智裕くん(博士後期課程2年)が、令和7年度 静岡大学大学院 光医工学研究科「成績優秀者」に選ばれました。
この制度は、研究成績が特に優れた大学院生(博士)に授与されるもので、日頃の研究活動と学問への真摯な取り組みが高く評価された結果です。今後のさらなる活躍が期待されます。

Organic Chemistry for Drug Discovery
当研究室の大学院生、竹尾沙優里さん(博士後期課程3年)、田口佳紀くん(博士後期課程3年)、飯尾智裕くん(博士後期課程2年)が、令和7年度 静岡大学大学院 光医工学研究科「成績優秀者」に選ばれました。
この制度は、研究成績が特に優れた大学院生(博士)に授与されるもので、日頃の研究活動と学問への真摯な取り組みが高く評価された結果です。今後のさらなる活躍が期待されます。

Adaptor-specific peptide inhibitors of the ubiquitin-chain-dependent unfolding activity of the human p97(VCP)–UFD1–NPL4 complex
Kei Okatsu1, Takaya Kawaguchi, Kohei Watanabe, Yoshinori Taguchi, Reon Takeuchi, Akinori Okamoto, Yasuyuki Iwasa, Takuya Tomita, Yasushi Saeki, Yusuke Sato,* Tetsuo Narumi,* & Shuya Fukai*

J. Med. Chem., 2025, 68, 11270.
The AAA-ATPase p97, a key component of the ubiquitin-proteasome system (UPS), collaborates with its cofactor, the UFD1–NPL4 (UN) heterodimer, to unfold ubiquitinated substrates leading to proteasomal degradation. In this study, we report the development of novel peptide inhibitors that specifically target the p97–UN complex. These inhibitors are designed based on the NPL4-binding motif (NBM) of UFD1 and disrupt the interaction between p97 and the UN heterodimer. Our results demonstrate that these peptides effectively inhibit the unfolding activity of p97–UN, suggesting their potential as a therapeutic strategy for diseases associated with UPS dysfunction, such as cancer and neurodegenerative disorders. This work provides the first mechanistic insights into the inhibition of p97–UN by high-affinity peptide inhibitors and introduces promising candidates for drug development targeting the stable p97–UN complex in cells.
竹田和真(M1)が 日本薬学会第145年会にて、学生優秀発表賞を受賞しました!

受賞した発表題目および学生は下記の通りです。
“HBVコアタンパク質由来ペプチドの変異解析によるHBVカプシド集合阻害剤の創製研究“
◯ 竹田和真, 竹尾沙優里, 佐藤浩平, 間瀬暢之, 中島謙治, 横山勝, 鈴木哲朗, 鳴海哲夫
今後も、研究室一同、優れた研究を追求してまいります。受賞した学生さん、おめでとうございます!今後の活躍にも期待しています。
Racemization-free peptide bond formation via 2-nitrobenzensulfonyl strategy for diastereoselective synthesis of (Z)-fluoroalkene- type peptidomimetics
Chihiro Iio, Kohei Sato, Nobuyuki Mase, and Tetsuo Narumi*

The Xaa-Pro-type (Z)-fluoroalkene dipeptide isostere (FADI) serves as a versatile surrogate for peptide bonds, effectively restricting cis–trans isomerization of the prolyl amide bond and offering advantages in the development of conformationally constrained peptide analogues. However, the diastereoselective synthesis of tripeptidomimetics incorporating Xaa-Pro-type FADIs is challenging due to the high susceptibility to racemization of the α-stereogenic center during peptide bond formation. Here, we introduce a racemization- and epimerization-free coupling strategy for the stereoselective synthesis of fluoroalkene-type peptidomimetics by reacting Xaa-Pro-type FADIs with amino acid benzyl esters or peptides. This approach leverages the unique properties of the 2-nitrobenzenesulfonyl (Ns) group as an N-terminal protecting group, which promotes sulfonamide anion formation, effectively suppressing α-deprotonation and thereby preventing racemization or epimerization. Our findings highlight the pivotal role of the N-Ns group in peptide synthesis and provide a robust platform for expanding the utility of FADIs in peptidomimetic designing.
田口佳紀(D2)が The 11th International Symposium toward the Future of Advanced Research at Shizuoka University 2025 にて、ベストプレゼンテーション賞を受賞しました!

受賞した発表題目および学生は下記の通りです。
“Chemical Synthesis of An Ester-to-Amide Analogue of Ester-linked Ubiquitin Dimer for Interactome Analysis”
◯ Yoshinori Taguchi, Takuya Tomita, Takuma Nishizawa, Dai Nakamura, Kohei Sato, Nobuyuki Mase, Yasushi Saeki and Tetsuo Narumi
今後も、研究室一同、優れた研究を追求してまいります。受賞した学生さん、おめでとうございます!今後の活躍にも期待しています。
Takuma Chizaki, Koichi Fujiwara, Junko Fujimoto, Tetsuo Narumi, Satoshi Shuto, and Mizuki Watanabe
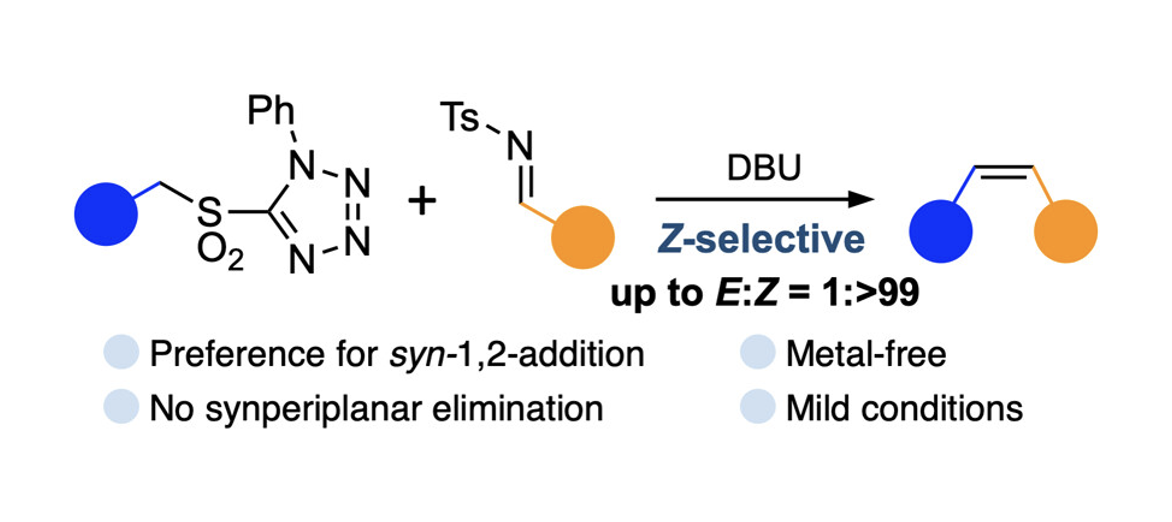
The Julia−Kocienski (JK) olefination is effective for E-selective olefination, but highly Z-selective versions remain rare. Here, we report a highly Z-selective JK olefination (Z ratio >99:1) using N-sulfonylimines as electrophiles instead of aldehydes. This method demonstrates a broad substrate scope, tolerating electron-donating and-withdrawing groups, amides, halogens, carboxylic acids, and hydroxyls. Z-selectivity in our system arises from both the 1,2-addition and Smiles rearrangement steps without involving synperiplanar elimination. This study expands the toolkit for Z-selective olefin synthesis.
恒例の「研究室旅行 in 京都」
今年は3/1から3/3までの2泊3日で京都に行ってきました。
新しく研究室配属されたB3や喜屋武 龍二先生(現 福山大薬助教)をはじめとしたOBの方々を含め総勢20名以上で京都観光しました!!
初日は、岡崎神社、一乗寺でラーメン、上賀茂神社へ。途中、田中智博先生(岡大院薬准教授)も合流し、源光庵 、今宮神社であぶり餅を堪能しました。
夜は四条で鳴海先生が学生時代から交流のある高山健太郎先生(京都薬大准教授)と小林数也先生(京都薬大准教授)も合流し、夕食を楽しみました。サプライズで修了するM2と卒業するB4をお祝いし、研究室を振り返ってもらいました!また、OBの方々から、鳴海研10周年のお祝いとして、鳴海先生へ記念パーカーとお花がプレゼントされました!
2日目はあいにくの曇天でしたが、北野天満宮、二条城、銀閣寺を散策し、お昼ごはんには鳴海先生が学生時代から通う大鵬に伺いました。
午後は、京山城屋にて「七味作り体験」を行い、各自オリジナルの七味を作りました!その後、八坂神社に移動して集合写真を撮影、夜はAce Cafeで鴨川の夜景を堪能しました。
最終日は、京都水族館で日本では珍しいオオサンショウオをはじめとして様々な海のいきものに触れました!
参加してくださった先生やOBの方々、ありがとうございました!
今年もみなさんありがとうございました!
